近日,山东大学高等医学研究院王维教授团队在Nature Communications期刊在线发表了题为“Trimbody with rigid AI-designed scaffolds enables atomic-resolution cryo-EM structure determination of small proteins”的研究论文。该研究设计出一种Trimbody通用性系统,实现了对小蛋白的原子分辨率冷冻电镜结构解析。山东大学高等医学研究院王维教授、自然资源部第三海洋研究所李增鹏教授、山东大学药学院侯旭奔教授为本文共同通讯作者。山东大学高等医学研究院博士生宋金扬、山东大学医学创新研究共享大平台主任齐磊为本文共同第一作者。
山东大学冷冻电镜平台为以上研究成果提供了关键硬件支持,特别是在冷冻样品制备、单颗粒数据收集和电镜数据三维重构方面发挥了重要作用,并重点提供了高分辨率数据收集服务。平台为该项研究制备了60个冷冻样品,并提供了长达20天的冷冻电镜机时,充分满足了研究团队对数据收集时间的需求。该研究共收集数据90 TB,这一庞大的数据集为后续的三维重构和结构分析奠定了坚实基础。
该项研究基于纳米抗体这一核心结合元件,通过RFdiffusion和ProteinMPNN等AI工具,从头设计出H3螺旋结构域与TAIL结构域,分别用于稳定纳米抗体与支架的结合并提升整体复合物的刚性,最终构建出由Nb-TAIL融合蛋白与H3-PrAC-5350A三聚体组成的Trimbody系统。该系统不仅结构简单、组装高效,而且通过引入AI设计的多重稳定界面,使纳米抗体与支架之间形成刚性连接,为靶蛋白冷冻电镜高分辨率解析创造了条件。Trimbody系统以其成本低廉、组装简单、与现有冷冻电镜工作流程的良好兼容性,为小分子量蛋白的高分辨率结构研究提供了新的通用工具,也为基于纳米抗体的药物研发及生命科学基础研究提供了重要支撑。
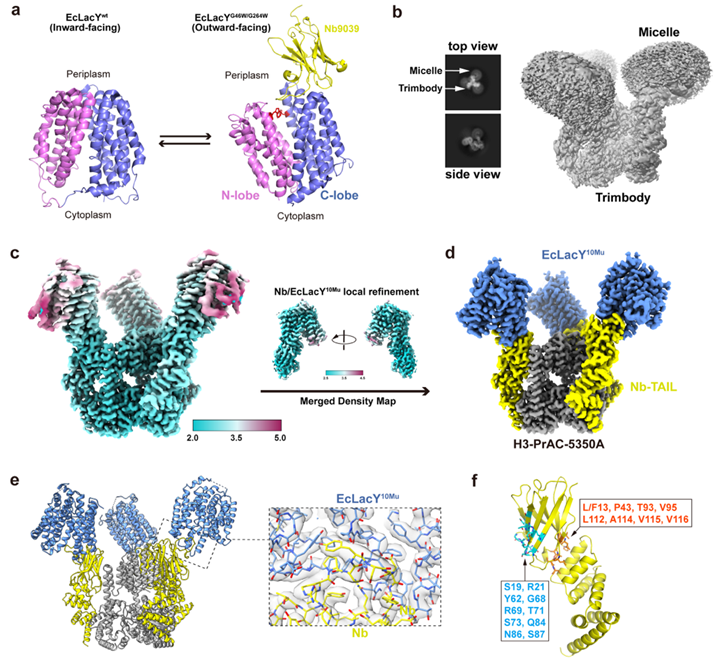
EcLacY10Mu/Trimbody复合物的冷冻电镜结构
原文链接:https://www.nature.com/articles/s41467-026-69941-9
此外,近期平台支撑的山东大学微生物改造技术全国重点实验室高翔团队的研究论文“Effector conformational plasticity enables lineage-specific secretion via Hcp heterohexamers in gut symbionts”也已在Nature Communications发表。该论文全面揭示了Hcp2/Hcp3异源六聚体特异性递送V1区效应蛋白的分子机制,证实了分子量较大的效应蛋白可通过构象变化适应狭窄Hcp内管进而被T6SS递送,突破了以往认为Hcp仅能递送较小分子量效应蛋白的观点,提出了Hcp变体与效应蛋白协同进化的“锁-钥”互作模型。该研究深化了对肠道菌群菌间竞争分子机制的理解,同时也为T6SS的工程化设计及潜在应用奠定了重要的结构及理论基础。
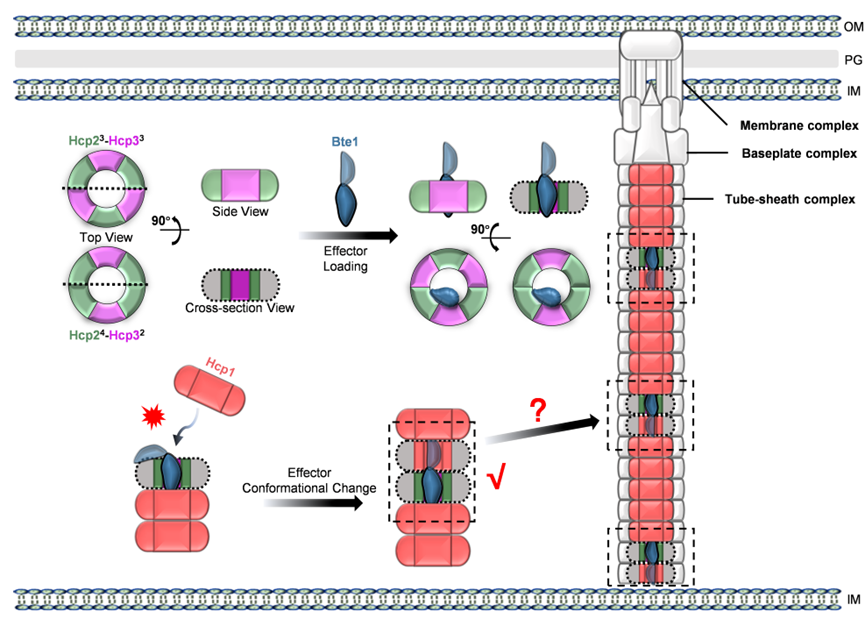
Hcp2-Hcp3异源六聚体递送V1区效应蛋白模式图
原文链接:https://www.nature.com/articles/s41467-026-69309-z
冷冻电镜平台旨在集中冷冻电镜技术优势资源,建成区域性开放共享的大型科研基地,已配备2台Krios G4 300kV冷冻电镜、1台Tundra 100kV冷冻电镜、1台Aquilos2冷冻双束电镜、若干制样设备和小型计算集群,具备冷冻样品制备、高分辨数据收集和三维结构解析全流程技术支撑能力,可为生物学、医学、药学和其他相关学科提供一流的分析测试。平台自2023年5月正式运行至今,已支撑发表SCI论文22篇,其中CNS 9篇,欢迎校内外师生咨询测试!
平台地址:山东省济南市历下区文化西路44号山东大学趵突泉校区冷冻电镜楼
联系电话:0531-88381105
